Surveillance environnementale : les installations de test pour la contamination en production
 janv., 12 2026
janv., 12 2026
Quand une usine de fabrication de médicaments, d’aliments prêts à la consommation ou de cosmétiques sort un produit, elle ne peut pas se permettre d’être à l’origine d’une contamination. Un seul pathogène mal détecté peut entraîner un rappel de produit, une perte de confiance, voire des hospitalisations. C’est pourquoi la surveillance environnementale n’est plus une option : c’est une exigence réglementaire, technique et éthique.
Comment la contamination se propage dans les installations de production
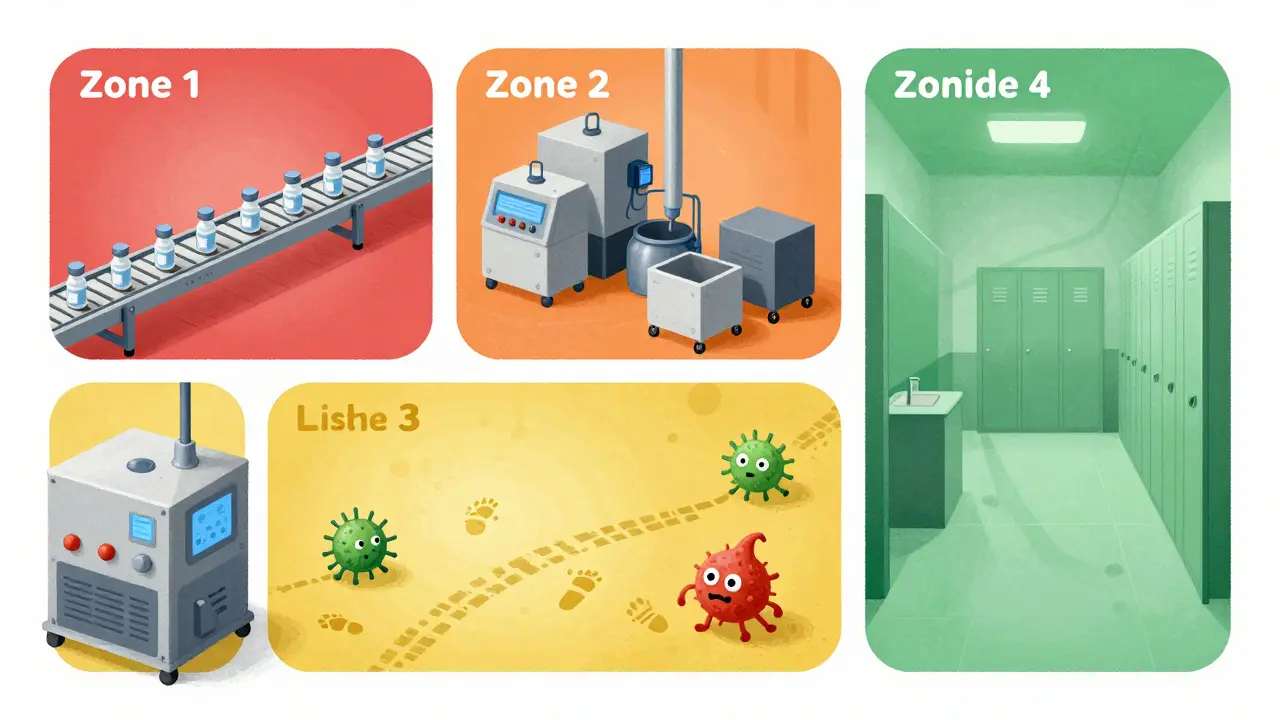
La contamination ne vient pas toujours de la matière première. Souvent, elle se niche dans les surfaces, l’air, les drains ou même les vêtements des opérateurs. Les micro-organismes comme Listeria monocytogenes ou Salmonella peuvent survivre des semaines sur des surfaces froides et humides. Les particules non viables - poussières, fibres, particules de peau - peuvent transporter des bactéries ou altérer la pureté d’un produit stérile. Les installations sont donc divisées en quatre zones de risque, un système universel adopté par l’industrie pharmaceutique, alimentaire et cosmétique. La Zone 1 inclut les surfaces en contact direct avec le produit : cuves, convoyeurs, couteaux de découpe, emballages. La Zone 2 regroupe les surfaces proches mais non en contact direct : les extérieurs des machines, les portes de réfrigérateurs, les chariots de transport. La Zone 3 couvre les zones plus éloignées mais encore dans l’aire de production : sols, tuyaux au-dessus des lignes, systèmes de ventilation. La Zone 4 est l’extérieur de la zone de production : vestiaires, couloirs, salles de repos. Un étude de PPD Laboratories (2010-2013) a révélé que 62 % des événements d’alerte provenaient des sols - c’est-à-dire de la Zone 3. Ce n’est pas la zone la plus visible, mais elle est la plus négligée. Et pourtant, un sol contaminé peut propager des agents pathogènes sur les roues des chariots, puis sur les équipements de la Zone 1.Les méthodes de test : de l’air aux surfaces
Les tests ne sont pas tous les mêmes. Ils dépendent du type de contaminant recherché. Pour les micro-organismes, on utilise des éponges stériles ou des coton-tiges pour prélever les surfaces. Ces échantillons sont ensuite incubés pendant 24 à 72 heures pour compter les colonies formant des unités (CFU). Pour l’air, on utilise des capteurs à impaction liquide ou solide. Ces appareils aspirent des volumes d’air importants - jusqu’à 1 000 litres - et capturent les particules sur des milieux de culture. Les résultats s’expriment en CFU par mètre cube d’air. Pour les métaux lourds, on utilise la spectrométrie par plasma couplé (ICP). Pour les composés chimiques, la chromatographie en phase gazeuse (GC) ou en phase liquide (HPLC) permet d’identifier des résidus de nettoyage ou des contaminants d’origine industrielle. Pour l’eau, on mesure la conductivité et le carbone organique total (TOC) - des indicateurs de pureté exigés par les normes USP <645> dans l’industrie pharmaceutique. Les tests rapides comme l’ATP (triphosphate d’adénosine) gagnent en popularité. Ils mesurent la présence de matière organique vivante en quelques secondes. Les usines qui les utilisent réduisent de 32 % le temps entre deux cycles de production, car elles n’attendent pas les résultats microbiologiques classiques. Mais l’ATP ne détecte pas les pathogènes spécifiques - seulement la présence de contamination globale. C’est un outil de vérification rapide, pas de diagnostic.Les réglementations qui dictent les pratiques
Les exigences varient selon le secteur, mais elles sont de plus en plus strictes. Dans l’industrie pharmaceutique, l’Annexe 1 de l’EMA (2023) exige une surveillance continue de la qualité de l’air dans les zones stériles. Les salles propres doivent maintenir un niveau ISO Class 5 - l’équivalent du grade B européen - avec un nombre maximum de particules non viables par mètre cube. Les températures et humidités sont enregistrées en temps réel. Dans l’industrie alimentaire, la règle Listeria (9 CFR part 430) de l’USDA oblige les fabricants d’aliments prêts à la consommation à tester hebdomadairement les Zones 1 et 2 pour Listeria monocytogenes. Selon les données de la FDA, 87 % des épidémies liées à la contamination environnementale auraient pu être évitées avec un bon programme de surveillance. La FDA et l’EMA exigent que les échantillons soient prélevés par du personnel formé. Une formation minimale de 40 heures en technique de prélèvement est recommandée. Beaucoup d’entreprises sous-estiment cet aspect : 68 % des sites enquêtés par l’IDFA en 2020 ont reconnu des erreurs dans la technique de prélèvement, comme l’utilisation d’éponges non stériles ou le non-respect des protocoles de stérilisation des appareils.
Les erreurs courantes et comment les éviter
Même les meilleures intentions peuvent échouer à cause de mauvaises pratiques. La première erreur : une classification des zones mal définie. Dans une usine, un tuyau au-dessus d’une ligne de production peut être considéré comme Zone 2 par un manager et Zone 1 par un autre, selon qu’il goutte ou non. Cette incohérence crée des failles. La solution ? Un document de classification signé par la qualité, la production et la sécurité, basé sur des observations réelles et non sur des hypothèses. La deuxième erreur : des fréquences de prélèvement arbitraires. Beaucoup de sites testent les Zones 3 et 4 une fois par mois, simplement parce que « c’est ce qu’on a toujours fait ». Mais si un sol est humide, proche d’un drain, et qu’il y a eu un débordement la semaine précédente, il doit être testé quotidiennement. La fréquence doit être basée sur le risque, pas sur le calendrier. La troisième erreur : la fragmentation des données. Les résultats de l’ATP, les tests microbiologiques, les analyses chimiques et les contrôles d’allergènes sont souvent stockés dans des systèmes différents. Résultat : personne ne voit le tableau complet. Les meilleurs sites utilisent des logiciels d’intégration qui fusionnent ces données pour détecter des tendances. Par exemple, une augmentation simultanée des CFU et des lectures ATP dans une zone peut signaler un problème de nettoyage récurrent.Coûts, ressources et retour sur investissement
Un programme de surveillance environnementale n’est pas bon marché. Une usine moyenne dépense entre 15 000 et 25 000 € par an en consommables, tests de laboratoire et formation. Elle consacre souvent 2 à 3 postes à temps plein à la surveillance. Mais le coût d’un échec est bien plus élevé. Un rappel de produit dans l’industrie alimentaire coûte en moyenne 10 millions de dollars aux États-Unis, selon l’USDA. Dans l’industrie pharmaceutique, un seul lot contaminé peut entraîner des pertes de plusieurs millions d’euros et une perte de licence. Les entreprises qui investissent dans la surveillance environnementale voient un retour sur investissement clair : moins de rappels, moins de retards de production, et une meilleure réputation. Les laboratoires qui utilisent des méthodes rapides comme l’ATP ou la séquençage de prochaine génération (NGS) réduisent le temps de libération des lots de 48 à 72 heures à moins de 24 heures - ce qui accélère la mise sur le marché.
Les tendances futures : intelligence artificielle et surveillance en temps réel
L’avenir de la surveillance environnementale est connecté. Depuis 2023, l’EMA exige que les installations pharmaceutiques intègrent la tendance des données en temps réel. Les capteurs d’air, de température et d’humidité envoient des données directement à des plateformes numériques. L’intelligence artificielle analyse ces données pour prédire les pics de contamination avant qu’ils ne se produisent. Par exemple, si la température d’un réfrigérateur monte légèrement pendant 3 heures, et que le taux de particules dans l’air augmente simultanément, l’IA peut alerter l’équipe de maintenance avant qu’un pathogène ne se développe. Les nouvelles méthodes de séquençage génétique permettent d’identifier un pathogène en moins de 24 heures, contre 3 à 5 jours auparavant. Cela permet de tracer la source exacte : est-ce une souche venue du sol ? Des vêtements ? Du personnel ? L’industrie est en train de passer d’une approche réactive - « on teste, on trouve, on nettoie » - à une approche prédictive - « on anticipe, on agit, on évite ».Que faire si vous démarrez un programme de surveillance ?
Commencez par définir vos zones. Ne vous fiez pas à l’intuition. Observez les flux de production, les points de condensation, les zones humides, les endroits où les équipements se touchent. Documentez chaque surface. Choisissez vos analytes en fonction de votre produit. Si vous fabriquez des aliments prêts à la consommation, concentrez-vous sur Listeria. Si vous produisez des injections stériles, surveillez les particules et les endospores. Formez votre équipe. Pas de tests sans formation. Utilisez des vidéos, des démonstrations en direct, et des audits croisés. Intégrez vos données. Un logiciel qui relie les tests microbiologiques, les lectures ATP et les contrôles de température est un investissement, pas un coût. Et surtout, testez régulièrement vos propres procédures. Un programme de surveillance qui n’est pas vérifié est un programme vide.Quelle est la différence entre une surveillance environnementale et un contrôle de qualité du produit ?
Le contrôle de qualité du produit vérifie si le produit fini répond aux spécifications. La surveillance environnementale vérifie si l’environnement de production est propre. C’est une prévention : si l’air, les surfaces et l’eau sont contrôlés, le produit a moins de chances d’être contaminé. Les deux sont nécessaires, mais la surveillance environnementale agit en amont.
Faut-il tester tous les jours dans la Zone 1 ?
Pas forcément. La fréquence dépend du risque. Pour un produit stérile ou un aliment prêt à la consommation, un prélèvement quotidien est souvent exigé. Pour d’autres produits, une fréquence hebdomadaire peut suffire si les données historiques montrent une stabilité. L’important est d’adapter la fréquence à la preuve - pas à la routine.
L’ATP peut-il remplacer les tests microbiologiques ?
Non. L’ATP détecte la matière organique totale, mais ne distingue pas les bactéries pathogènes des bactéries inoffensives. Il est utile pour vérifier la qualité du nettoyage rapidement, mais ne peut pas remplacer les tests microbiologiques pour confirmer l’absence de Listeria ou de Salmonella. Les deux sont complémentaires.
Pourquoi les sols sont-ils souvent la source de contamination ?
Les sols sont des zones de passage pour les chariots, les chaussures, les outils et l’air. Ils sont souvent moins nettoyés que les surfaces de production, et peuvent accumuler de l’humidité, des débris organiques et des pathogènes. Une étude a montré que 62 % des événements de contamination venaient des sols - ce qui prouve qu’on ne peut pas les négliger.
Quels sont les signes qu’un programme de surveillance est inefficace ?
Des résultats sporadiques sans tendance claire, des écarts entre les zones, des tests qui ne sont jamais suivis d’actions correctives, ou des données isolées dans des fichiers Excel. Un bon programme génère des tendances, des alertes précoces, et des actions concrètes. S’il ne fait que remplir des formulaires, il ne sert à rien.
Frédéric Nolet
janvier 13, 2026 AT 01:57Franchement, j’ai vu des usines où ils testaient les sols une fois par mois… et puis un jour, 3 lots contaminés en 2 semaines. Après ça, ils ont passé à du quotidien. La surveillance, c’est pas un check-box, c’est une culture.
Charles Goyer
janvier 14, 2026 AT 16:4062 % des contaminations viennent des sols ? Ben non, ça vient des managers qui croient que ‘on a toujours fait comme ça’ suffit. La science, c’est pas une tradition de famille.
jacques ouwerx
janvier 16, 2026 AT 04:47Vous savez quoi ? Moi j’ai travaillé dans une usine de cosmétiques, on utilisait l’ATP tout le temps. C’était super rapide, mais après, faut quand même confirmer avec les cultures. Sinon, tu penses que tout est propre… et t’as une surprise le lendemain. 😅
armand bodag
janvier 16, 2026 AT 21:41La surveillance environnementale, c’est juste une manière de justifier des coûts aux actionnaires. Le vrai problème, c’est que l’industrie préfère payer pour un rappel qu’investir dans la prévention. C’est le capitalisme, pas la science.
Arnaud Bourgogne
janvier 18, 2026 AT 06:07Vous croyez que c’est pour la santé ? Non. C’est pour que les grandes entreprises écrasent les PME. Les normes sont trop chères pour les petits. C’est un complot pour contrôler l’industrie. La FDA et l’EMA, c’est la même boîte.
Marie Linne von Berg
janvier 19, 2026 AT 03:24Je suis super contente de voir que les gens commencent à comprendre l’importance des zones ! 🙌 Et surtout, la formation ! J’ai vu des techniciens qui utilisaient des éponges non stériles… j’ai failli pleurer. 💔 Formez vos équipes, c’est le vrai ROI !
Danielle Bowern
janvier 20, 2026 AT 12:10le truc avec les sols c’est qu’on les oublie parce qu’on les voit pas comme une menace directe… mais c’est là que tout commence. un chariot qui passe, une chaussure qui traîne… et hop. la contamination est là. c’est fou comment on sous-estime les choses simples
James Fitzalan
janvier 20, 2026 AT 12:35Je vous dis qu’on est en train de vivre une révolution. L’IA va tout changer. Dans 5 ans, on va plus avoir de techniciens qui prélèvent des échantillons. Des capteurs, des algorithmes, et un signal d’alerte avant même qu’un humain le voie. C’est la fin de l’ère du papier et du stylo.
Jean-Pierre Vanfürt
janvier 21, 2026 AT 04:34Vous savez ce qu’ils font dans les labos ? Ils trichent. Ils mettent les échantillons dans des salles propres avant de les analyser. Les résultats sont bidonnés. Les normes sont un leurre. Les régulateurs sont complices. C’est un système corrompu.
Mathieu MARCINKIEWICZ
janvier 22, 2026 AT 08:13je viens de lire tout ca et j’ai juste envie de dire merci. c’est rare qu’on explique aussi clairement pourquoi les sols comptent. j’ai un pote qui travaille dans une usine et il me disait que c’était ‘trop cher’ de faire des tests quotidiens… j’ai pu lui envoyer cet article. il a changé d’avis. c’est cool
André Dellara
janvier 23, 2026 AT 03:33Il convient de souligner, avec la plus grande rigueur, que la classification des zones de risque doit être documentée, validée, et soumise à une révision périodique, conformément aux exigences de l’Annexe 1 de l’EMA, ainsi qu’aux bonnes pratiques de fabrication (GMP) telles que définies par l’OMS et la FDA. Toute déviation constitue un non-conformité majeure.
Jacque Meredith
janvier 24, 2026 AT 00:26Vous avez tous tort. Le vrai problème, c’est que personne ne contrôle les fournisseurs de matériel de prélèvement. Les éponges, les coton-tiges… ils sont contaminés dès la sortie d’usine. C’est une fraude systémique.